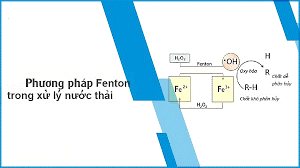
XỬ LÝ NƯỚC THẢI BẰNG PHƯƠNG PHÁP FENTON – OXY HÓA BẬC CAO
Trong bối cảnh các quy chuẩn xả thải ngày càng nghiêm ngặt, nhiều loại nước thải công nghiệp chứa hợp chất hữu cơ khó phân hủy sinh học không thể xử lý triệt để bằng các phương pháp truyền thống. Khi đó, phương pháp Fenton – oxy hóa bậc cao (AOP) được xem là giải pháp hiệu quả, đặc biệt ở giai đoạn tiền xử lý.
Phương pháp Fenton sử dụng phản ứng giữa hydrogen peroxide (H₂O₂) và ion sắt (Fe²⁺) để tạo ra *gốc hydroxyl (OH) – một trong những tác nhân oxy hóa mạnh nhất hiện nay, có khả năng phá hủy hầu hết các hợp chất hữu cơ độc hại.
1. Phương pháp Fenton là gì?
Xử lý nước thải bằng phương pháp Fenton là một dạng công nghệ oxy hóa bậc cao (Advanced Oxidation Processes – AOPs), thường được áp dụng trong:
-
Giai đoạn tiền xử lý
-
Hoặc xử lý nâng cao trước sinh học / sau sinh học
Phương pháp này đặc biệt hiệu quả với nước thải chứa:
-
Hợp chất hữu cơ khó phân hủy
-
Màu, COD cao
-
Chất độc hại bền vững
👉 Các ngành ứng dụng phổ biến: dệt nhuộm, giấy, hóa chất, xi mạ, thuộc da.
2. Nguyên lý oxy hóa bậc cao của công nghệ Fenton
Công nghệ Fenton dựa trên việc tạo ra *gốc tự do hydroxyl (OH) thông qua phản ứng giữa Fe²⁺ và H₂O₂.
🔹 Gốc *OH có đặc tính:
-
Thế oxy hóa rất cao (~2,8 V)
-
Phản ứng nhanh
-
Không chọn lọc
Nhờ đó, *OH có thể:
-
Phá vỡ cấu trúc các hợp chất hữu cơ phức tạp
-
Chuyển chúng thành CO₂, H₂O hoặc các acid hữu cơ mạch ngắn
-
Giảm mạnh COD, màu và độc tính nước thải
3. Quy trình xử lý nước thải bằng phương pháp Fenton
3.1 Điều chỉnh pH
pH ảnh hưởng trực tiếp đến:
-
Tốc độ phản ứng
-
Trạng thái tồn tại của ion sắt
👉 pH thích hợp cho phản ứng Fenton:
-
Khoảng: 2 – 4
-
Tối ưu nhất: ~2,8
3.2 Giai đoạn phản ứng oxy hóa
Phản ứng tạo gốc hydroxyl diễn ra theo phương trình:
*Fe²⁺ + H₂O₂ → Fe³⁺ + OH⁻ + OH
Gốc *OH sẽ oxy hóa các hợp chất hữu cơ:
*CHC (cao phân tử) + OH → CHC (thấp phân tử) + CO₂ + H₂O + OH⁻
👉 Kết quả:
-
Phân hủy các chất hữu cơ khó xử lý
-
Giảm COD, màu và độc tính
3.3 Trung hòa và keo tụ
Sau giai đoạn oxy hóa:
-
pH được nâng lên > 7
-
Fe³⁺ kết tủa thành Fe(OH)₃
Phản ứng:
Fe³⁺ + 3OH⁻ → Fe(OH)₃
Kết tủa Fe(OH)₃:
-
Hoạt động như chất keo tụ
-
Hấp phụ thêm các hợp chất hữu cơ còn sót lại
-
Tạo bông cặn dễ lắng
4. Các yếu tố ảnh hưởng đến hiệu quả phản ứng Fenton
Hiệu quả xử lý phụ thuộc vào nhiều yếu tố kỹ thuật:
🔹 Nồng độ ion sắt (Fe²⁺)
-
Là chất xúc tác tạo gốc *OH
-
Quá thấp → phản ứng kém
-
Quá cao → tiêu hao *OH, giảm hiệu quả
🔹 Nồng độ H₂O₂
-
Cung cấp nguồn tạo gốc hydroxyl
-
Dư thừa H₂O₂ → phản ứng phụ, giảm hiệu suất
🔹 pH dung dịch
-
Yếu tố quan trọng nhất
-
pH tối ưu: 2 – 4
🔹 Nhiệt độ và thời gian phản ứng
-
Nhiệt độ tăng → phản ứng nhanh hơn
-
Thời gian phụ thuộc vào mức độ ô nhiễm của nước thải
5. Ứng dụng của phương pháp Fenton trong xử lý nước thải
Nhờ hiệu quả oxy hóa mạnh, công nghệ Fenton được ứng dụng rộng rãi trong:
-
✔️ Xử lý nước thải dệt nhuộm (màu, COD cao)
-
✔️ Xử lý nước thải ngành giấy
-
✔️ Xử lý nước thải xi mạ
-
✔️ Xử lý nước thải hóa chất
-
✔️ Tiền xử lý trước sinh học để tăng khả năng phân hủy
👉 Tùy theo đặc tính nước thải đầu vào, kỹ sư sẽ thiết kế liều lượng hóa chất và quy trình phù hợp nhằm tối ưu chi phí – đảm bảo hiệu quả xử lý.